Klassifisering
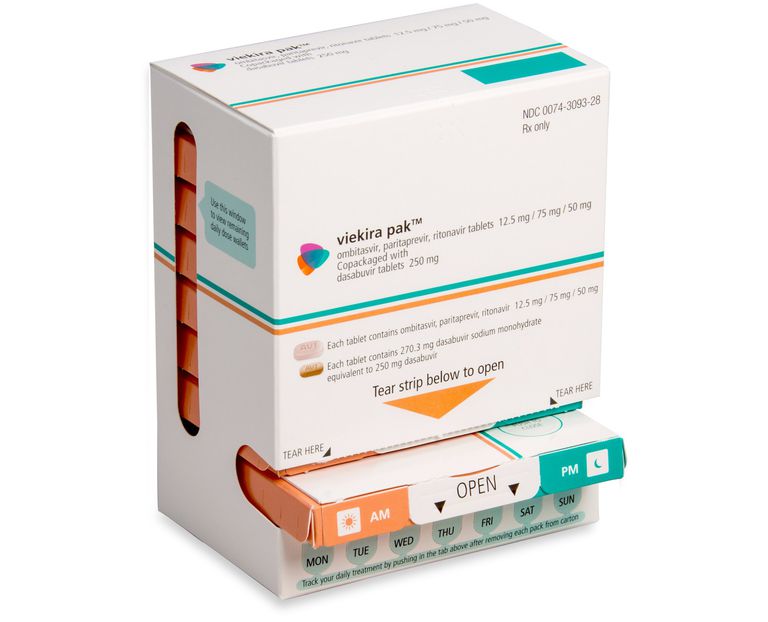
Viekira Pak er en kompaktpakket kombinasjon som brukes til behandling av kronisk hepatitt C (HCV) infeksjon. Pakken inneholder en kombinasjon med kombinasjonsdoser Technivie (ombitasvir + paritaprevir + ritonavir) kombinert sammen med stoffet dasabuvir.
Medikamentkomponentene ombitasvir, paritaprevir og dasabuvir er direktevirkende antivirale midler (DAAs) som forstyrrer replikasjonen av viruset.
Medikament ritonavir, som brukes ofte i HIV-terapi, er inkludert for å øke paritaprevirs narkotika nivå.
Viekira Pak er oftest, men ikke alltid, samtidig administrert med ribavirin og trenger ikke tas med pegylert interferon (peg-interferon). Viekira Pak ble godkjent 19. desember 2014 av US Food and Drug Administration (FDA) for bruk hos voksne 18 år eller eldre med HCV-genotypene 1-infeksjon, inkludert de med kompensert cirrhose (hvor leveren fortsatt fungerer) og levertransplantasjoner. For pasienter med dekompensert cirrhosis, anbefales ikke Viekira Pak.
Viekira Pak er rapportert å ha en kur på 95% eller mer, med kun 2% av pasientene som avslutter behandlingen på grunn av intoleranse. Det er hensiktsmessig for bruk hos pasienter med HIV / HCV-samtidig infeksjon.
Dosering
To tabletter av samformulerte tabletter av ombitasvir + paritaprevir + ritonavir (25 mg / 150 mg / 100 mg) tatt en daglig om morgenen med mat, samt ett tablett med dasabuvir tatt to ganger daglig om morgenen og kvelden med mat.
Tablettene kommer beleilig sammen i daglige doser med dosering, med doseringsinstruksjoner som følger med på hver boks. Den sammensatte tabletten er rosa, filmdrasjert og preget med "AV1", mens dasabuvir tablett er beige, filmdrasjert og preget med "AV2".
Prescribing Anbefalinger
Viekira Pak er foreskrevet i løpet av 12 til 24 uker i henhold til følgende anbefalinger:
Genotype 1a uten cirrhose: Viekira Pak med ribavirin i 12 uker
- Genotype 1a med cirrhosis: Viekira Pak med ribavirin i 24 uker
- Genotype 1b uten cirrhosis: Viekira Pak alene i 12 uker
- Genotype 1b uten cirrhosis: Viekira Pak med ribavirin i 24 uker
- For levertransplantasjonspatienter kan Viekira Pak kun tas med ribavirin i 24 uker bare hvis leverfunksjonen er normal og fibrose (arrdannelse) er mindre.
Vanlige bivirkninger
De vanligste bivirkningene ved bruk av Viekira Pak (forekommer hos opptil 10% av pasientene) er:
Utmattelse
- Kvalme
- Kløende hud
- Hudreaksjoner
- Søvnløshet Svakhet og tretthet
- Narkotikainteraksjoner
- Den Følgende bør også unngås ved bruk av Viekira Pak:
Antikonvulsiver: karbamazepin, fenytoin, fenobarbital
Antihyperlipidemika (brukes til å redusere lipidnivåer i blodet): gemfibrozil
- Anti-arytmiemedisin: pimozid
- Kolesterolreduserende medisin: lovastatin, simvastatin
- Erektil dysfunksjonsmedisin: Viagra (sildenafil)
- Ergotholdig medisin (brukes til å behandle hodepine og migrene): ergotamin, dihydroergotamin, ergonovin, metylergonovin
- Etinylestradiol (en menneskeskapte form for østrogen)
- HIV-medisinering: Sustiva (efavirenz), Atripla (efavirenz + tenofovir + emtricitabin)
- Hypotensjonsmedikamenter: alfuzosin
- Rifampinbasert anti-tuberkulose medisiner: Mycobutin, Rifater , Rifamate, Rimactane, Rifadin, Priftin
- Sedativer: triazolam, oral midazolam
- Kontraindikasjoner og overveielser
- For pasienter med moderat nedsatt leverfunksjon, anbefales ikke Viekira Pak. Viekira Pak er kontraindisert for bruk hos pasienter med alvorlig nedsatt leverfunksjon.
Viekira Pak er også kontraindisert for bruk hos pasienter med kjent overfølsomhet overfor ritonavir (inkludert Stevens-Johnsons syndrom, en potensielt livstruende, inflammatorisk reaksjon i hele kroppen).
Viekira Pak er kontraindisert for bruk hos gravide kvinner når de brukes sammen med ribavirin.
Det anbefales at alle kvinner i barnealderen overvåkes månedlig for graviditet i løpet av behandlingen. Det anbefales også at pasienten og hennes mannlige partner blir gitt minst to ikke-hormonelle prevensjonsmetoder, og at de skal brukes i løpet av behandlingen og i seks måneder etterpå.