Selv om onkologer i mange tilfeller kan ha gode verktøy og data for å sortere ut og sammenligne ulike behandlinger, kan nyutviklede terapier noen ganger være vanskelig å forutsi, uten klinisk erfaring.
Forskudd i kunnskap kommer fra kliniske studier, hvor pasientene er enige om å gå inn i studier med forskningsmedisiner som har vist noe løfte; men som begrepet "rettssaken" innebærer, er det alltid en viss grad av usikkerhet om hvor godt et stoff vil utføre og som vil ha mest nytte, det vil si hvilken pasienttyper og hvilke undergrupper av kreft. Hva er kreftimmunoterapi?
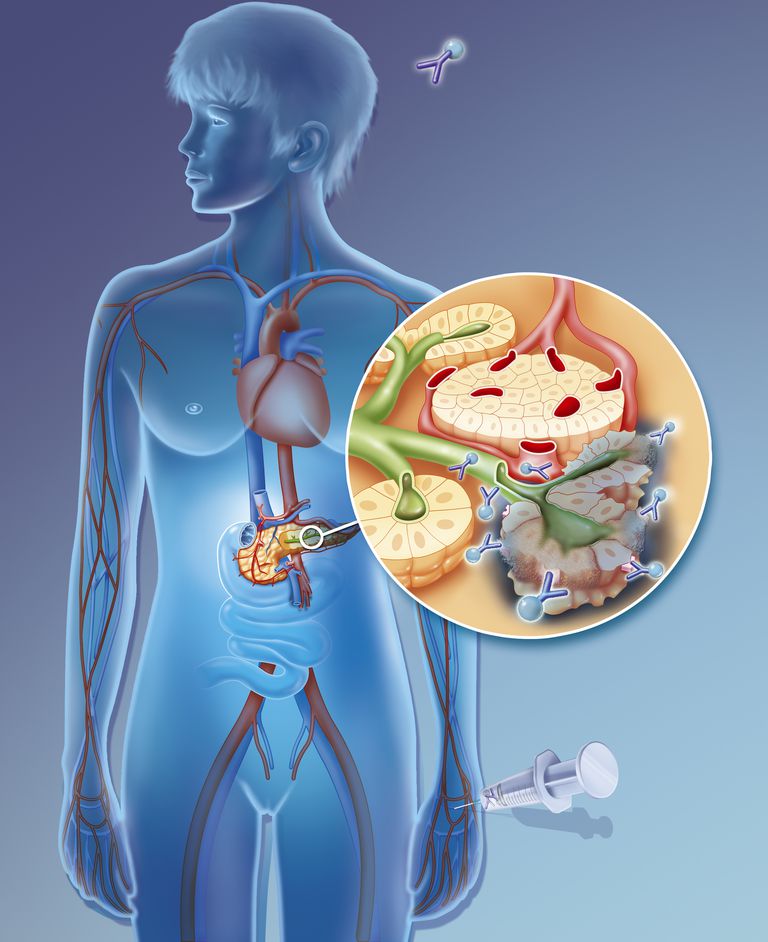
Kreft immunterapi er en behandling som involverer visse deler av individets immunsystem for å bekjempe maligniteten. Et eksempel på immunterapi er bruk av monoklonale antistoffer som rituximab og obinutuzumab. Monoklonale antistoffer er menneskeskapte antistoffer, eller immunsystemproteiner. Disse antistoffene kan angripe en svært spesifikk del av en kreftcelle i det som kalles målrettet terapi.
Andre former for kreftimmunterapi inkluderer immune kontrollpunktshemmere, som tar "bremser" av immunsystemet for å hjelpe det å gjenkjenne og angripe kreftceller.
Verden av kreftimmunterapi er på ingen måte begrenset til eksemplene ovenfor, og nye ideer for bruk av kroppens eget immunsystem for å bekjempe kreftcellene fortsetter å bli utviklet og testet.
Fungerer immunterapi for alle kviser?
Hver person er unik, og hver persons kreft er unikt; ikke alle reagerer på samme måte som den samme immunterapien.
Effektivt måling på forhånd, hvilke personer som mest sannsynlig vil reagere på en immunterapi, vil være fordelaktig fra flere vinkler. For pasienten kan det spare viktig tid, noe som kan oversette til klinisk fordel.
Med andre ord, ville du ikke kaste bort tiden din eller risikoen bivirkninger prøver noe som sannsynligvis vil ha en minimal effekt når det kan være en "større pistol" eller mer effektiv terapi tilgjengelig. Men hvordan kan man vite denne typen ting på forhånd? En historie om hvordan onkologer og kreftforskere går om å gjøre dette, begynner med noe som heter neoantigener.
Neoantigener: Kreftens Achilles Heal?
Kreftceller kan være sneaky. De har ofte en rekke forandringer i sine gener, hvorav noen kan korrespondere med deres evne til å gjøre dårlige ting som normale, friske celler ikke kan. Noen av disse endringene resulterer faktisk i fysiske forskjeller i eller på utsiden av kreftcellene som kan oppdages av immunsystemet. Disse delene av kreftceller som immunforsvaret kan gjenkjenne som utenlandske kalles "neoantigener". Neo, noe som betyr nytt, fordi de oppstår nylig fra
våre egne celler, har gått bort med kreft
, i motsetning til de vanlige antigenene forskerne snakker vanligvis om i smittsomme sykdommer, for eksempel.
Vanlige antigener kan finnes på utsiden av bakterier, eller virusinfiserte celler, for eksempel. I kontrast er neoantigener som røde flagg som kan signalere immunforsvaret som våre egne celler misforstår. Neoantigener fører til aktivering av hvite blodlegemer kjent som T-celler – immunsystemets soldater. Disse soldat-T-cellene reiser deretter blodkarene, som de antikke romene i antikke Roma, for å nå stedet for de urettmessige ondartede cellene, infiltrere svulsten og bidra til å avkrefte lokalbefolkningen av ondartede celler.Så neoantigener er en av nøklene til immunbasert anti-kreftbehandling.
Som sagt, å vinne slaget involverer sjelden immunterapi alene, og det er vanligvis behov for en mer brennstofftype tilnærming; immunoterapi brukes ofte i forbindelse med cytotoksisk kjemoterapi og / eller og andre immunoterpier, avhengig av malignitet og den enkelte pasient.
Vil immunterapi virke for meg?
Dette er et viktig spørsmål i moderne onkologi, og en som jobber aktivt. Mot den enden kan to karakteristika av kreftcellene hjelpe leger til å forutsi hvor godt tilgjengelig immunterapier vil fungere: TMB og MSI.
Tumor mutasjonsbelastning, eller
TMB
, kan betraktes som en indeks for alle de forandringene i gener i kreftcellene som har gått galt, for eksempel, som pleide å kode for alle de normale tingene en celle måtte trenge – men som har endringer eller mutasjoner i tilfelle av kreftceller. TMB er også ofte referert til som total mutasjonsbelastning eller mutasjonsbelastning.
Tumorer som har høy TMB antas å ha mer neoantigener og kan derfor reagere bedre på immunterapi. Kreftceller kan ende opp med høy TMB gjennom eksponeringer knyttet til kreft, inkludert tobakk eller UV-lys. En annen måte er gjennom mikrosatellitt ustabilitet, eller MSI, et teknisk begrep som refererer til et problem med kroppens naturlige mekanismer for DNA-reparasjon – et problem som resulterer i svært endrede og inkonsekvente lengder av repeterende DNA-gensekvenser.
Ett selskap kalt Foundation Medicine tilbyr nå de første fullstendig integrerte, validerte vurderingene av TMB som en del av FoundationOne-analysen, noe som kan bidra til å forutsi en persons potensielle respons på immunterapi. "Feilfulle genomene er fellesnevneren av alle kreftformer," forklarer Vincent Miller, MD, sjefleder ved Stiftelsesmedisin. "Tumorer med et spesielt høyt antall mutasjoner er mer sannsynlig å produsere nye, unormale proteiner kalt neoantigener. Immunsystemet gjenkjenner disse neoantigenene som fremmede og fortsetter å være høyt varslet og initierer en kompleks serie av trinn for å angripe svulsten. "Vil en immune kontrollpunktsinhibitor virke for meg?
Plottet fortykkes ved at enkelte kreftformer har utviklet ekstremt lurefulle måter å unnslippe immunsystemet ved å lage proteiner som faktisk inaktiverer visse typer immunceller. En biologisk avkjøling, hvis du vil.
For å hindre at kreft kommer fra seg selv på denne måten, har noen immunterapier blitt utformet for å blokkere disse immunforsvarende proteiner. Disse immunoterapiene, kjent som
immun-kontrollpunktshemmere
, inkluderer de betegnet anti-PD1- og anti-PDL1-antistoffer. Og, som med andre typer immunterapi, er det bevis som tyder på høyere nivåer av neoantigener i kreftcellene, som er forbundet med bedre responser på immune kontrollpunktshemmere. Responsen på kontrollpunktsinhibitorer varierer fra ca. 20 prosent i lungekreft til 80 prosent i Hodgkin lymfom. Årsaken til at visse svulster reagerer på kontrollpunktsinhibitorer, og andre er ikke uklare. Betydningen av å forutsi klinisk respons
Disse prediktive verktøyene og deres suksess var et tema for samtalen på årets møte i American Society of Clinical Oncology, eller ASCO. TMB har vist seg å forutse en større sannsynlighet for respons og lengre varighet av respons på kreftimmunoterapier hos pasienter med blærekreft, lungekreft, melanom og andre avanserte kreftformer. I tillegg til TMB måler FoundationOne også mikrosatellitt ustabilitet, som representerer en enkelt test for å veilede terapeutiske beslutninger for målrettede terapier, kliniske studier og FDA-godkjente kreftimmunoterapier ved bruk av en enkelt biopsi."Kreftimmunoterapier står i forkant av kreftbehandling, og nye, kvantitative tilnærminger er nødvendige for å forutsi kliniske responser på denne viktige, men også dyre, klassen av terapier," sa Dr. Miller.
"Muligheten til å måle flere biomarkører samtidig, inkludert TMB og MSI, er et viktig fremskritt for kreftimmunterapi, og en som er unik for grunnmedisin," sa Thomas George, MD, GI onkologi programdirektør, University of Florida. "Foundation Medicine kombinasjon av avanserte sekvenseringsplattformer og svært spesifikke algoritmer gir meg tilgang til alle relevante genomiske biomarkører for mine pasienter samtidig, noe som bidrar til å spare både tid og vev."
"Vi ble oppmuntret av funnene presentert ved ASCO, inkludert muligheten for å identifisere pasienter som er mer sannsynlig å dra nytte av kontrollpost inhibitor immunterapi," sa Dr. Miller. "Vårt mål er å styrke leger og pasienter med et bredt spekter av relevante, gjennomførbare genomiske opplysninger, og vi er glade for å tilby vår særegne løsning for å estimere TMB og MSI samtidig og med eksepsjonell nøyaktighet, støttet av sofistikerte algoritmer og forankret i kontekstuell innsikt fra vår kunnskapsbase FoundationCORE. Dette er noe ingen andre neste generasjons sekvenseringsplattform tilbyr. "
Uavhengig av FoundationOne og FoundationOne Heme-analysene, tilbyr Foundation Medicine også testing for PD-1 og PD-L1 proteinuttrykk, og gir, i kombinasjon med FoundationOne-analysene, en fullstendig suite av kreft immunterapi analyser for onkologer.
Et ord fra Verywell
Selv om dette er absolutt et lovende område, utvikler vitenskapen seg fortsatt og ulike tester blir fortsatt studert og validert. Alle nåværende biomarkører for prediksjon av klinisk respons til kontrollpunktsinhibitorer er bare undersøkelser, og det finnes for øyeblikket ingen FDA-godkjente tester som kan forutsi nøyaktig responsen til å kontrollere punkthemmere.

